Аварийно химические опасные вещества
Аварийно химические опасные вещества (аммиак, хлор). Их воздействие на организм человека. Предельно допустимые и поражающие концентрации
Растет ассортимент применяемых в промышленности, сельском хозяйстве и быту химических веществ. Некоторые из них токсичны и вредны. При проливе или выбросе в окружающую среду способны вызвать массовые поражения людей, животных, приводят к заражению воздуха, почвы, воды, растений. Их называют аварийно химические опасные вещества(АХОВ). Определенные виды АХОВ находятся в больших количествах на предприятиях, их производящих или использующих в производстве. В случае аварии может произойти поражение людей не только непосредственно на объекте, но и за его пределами, в ближайших населенных пунктах.
Крупными запасами опасных веществ располагают предприятия химической, целлюлозно-бумажной, оборонной, нефтеперерабатывающей и нефтехимической промышленности, черной и цветной металлургии, промышленности минудобрений.
Значительные их количества сосредоточены на объектах пищевой, мясо-молочной промышленности, холодильниках, торговых базах, различных АО, в жилищно-коммунальном хозяйстве.
Наиболее распространенными из них являются хлор, аммиак, сероводород, двуокись серы (сернистый газ), нитрил акриловой кислоты, синильная кислота, фосген, метилмеркаптан, бензол, бромистый водород, фтор, фтористый водород.
Хлор
При нормальных условиях газ желто-зеленого цвета с резким раздражающим специфическим запахом. При обычном давлении затвердевает при -101 °С и сжижается при -34° С. Тяжелее воздуха примерно в 2,5 раза. Вследствие этого стелется по земле, скапливается в низинах, подвалах, колодцах, тоннелях.
Ежегодное потребление хлора в мире достигает 40 млн. т.
Используется он в производстве хлорорганических соединений (винил хлорида, хлоропренового каучука, дихлорэтана, хлорбензола и др.). В большинстве случаев применяется для отбеливания тканей и бумажной массы, обеззараживания питьевой воды, как дезинфицирующее средство и в различных других отраслях промышленности.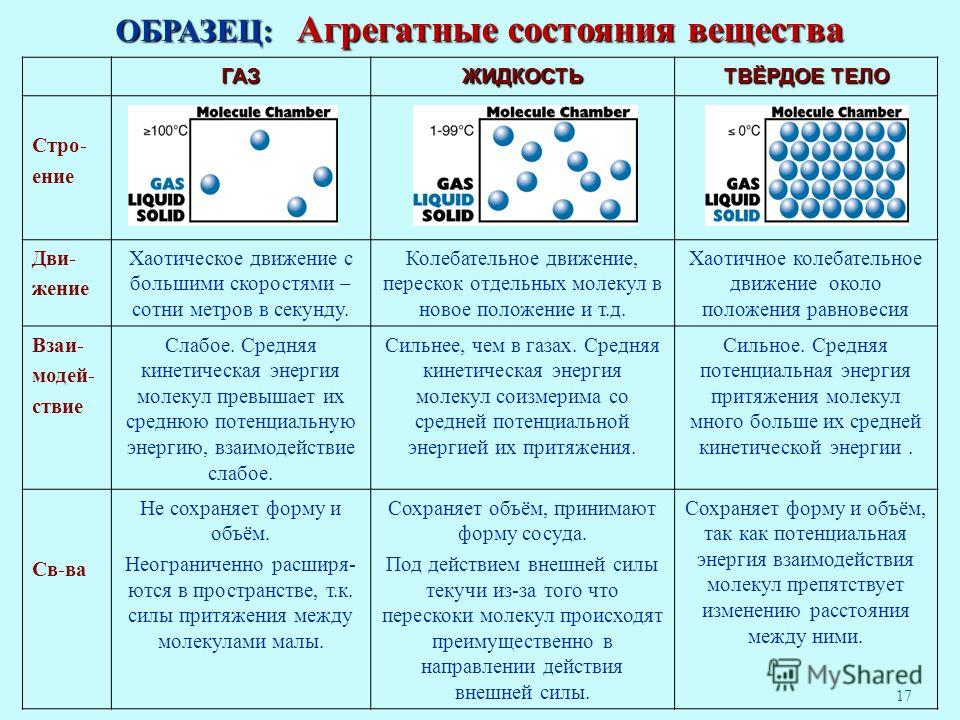
Хранят и перевозят его в стальных баллонах и железнодорожных цистернах под давлением. При выходе в атмосферу дымит, заражает водоемы.
В первую мировую войну применялся в качестве отравляющего вещества удушающего действия. Поражает легкие, раздражает слизистые и кожу.
Первые признаки отравления — резкая загрудинная боль, резь в глазах, слезоотделение, сухой кашель, рвота, нарушение координации, одышка. Соприкосновение с парами хлора вызывает ожоги слизистой оболочки дыхательных путей, глаз, кожи.
Воздействие в течение 30 — 60 мин при концентрации 100 — 200 мг/м3 опасно для жизни.
Если все-таки произошло поражение хлором, пострадавшего немедленно выносят на свежий воздух, тепло укрывают и дают дышать парами спирта или воды.
При интенсивной утечке хлора используют распыленный раствор кальцинированной соды или воду, чтобы осадить газ. Место разлива заливают аммиачной водой, известковым молоком, раствором кальцинированной соды или каустика с концентрацией 60 —80% и более (примерный расход — 2л раствора на 1 кг хлора).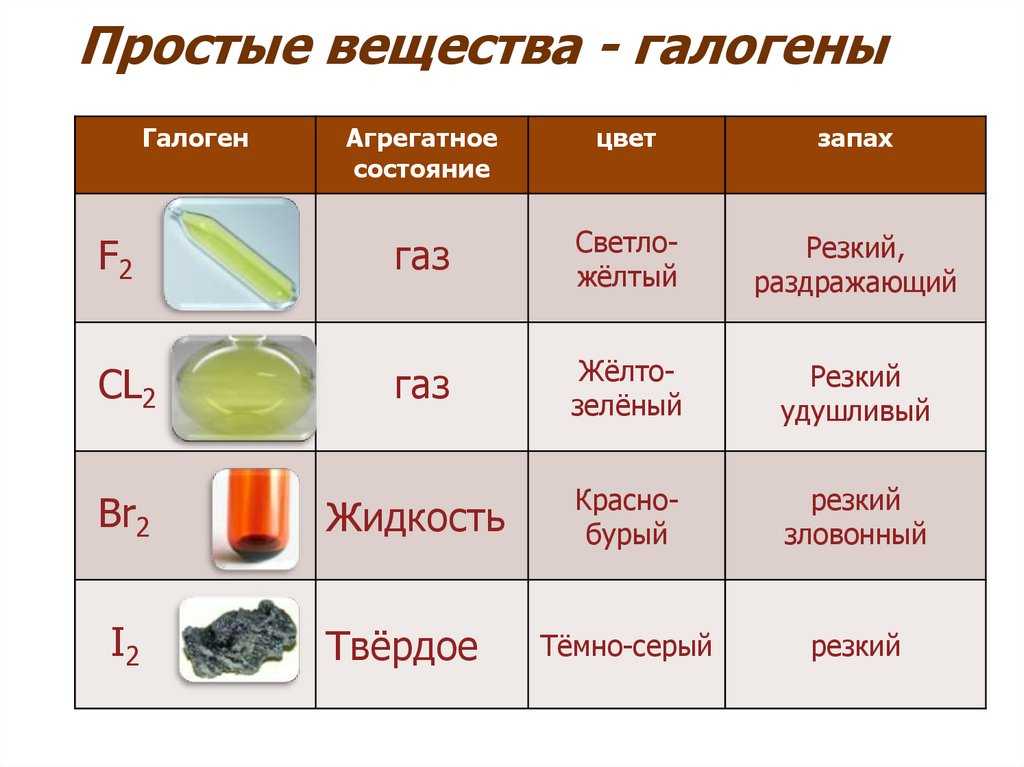
Аммиак
При нормальных условиях бесцветный газ с характерным резким запахом («нашатырного спирта»), почти в два раза легче воздуха. При выходе в атмосферу дымит. При обычном давлении затвердевает при температуре -78°С и сжижается при -34°С. С воздухом образует взрывоопасные смеси в пределах 15 — 28 объемных процентов.
Растворимость его в воде больше, чем у всех других газов: один объем воды поглощает при 20°С около 700 объемов аммиака, 10%-й раствор аммиака поступает в продажу под названием «нашатырный спирт». Он находит применение в медицине и в домашнем хозяйстве (при стирке белья, выведении пятен и т.д.). 18-20%-й раствор называется аммиачной водой и используется как удобрение.
Жидкий аммиак — хороший растворитель большинства органических и неорганических соединений.
Мировое производство аммиака ежегодно составляет около 90 млн.т. Его используют при получении азотной кислоты, азотосодержащих солей, соды, мочевины, синильной кислоты, удобрений, диазотипных светокопировальных материалов. Жидкий аммиак широко применяется в качестве рабочего вещества (хладагента) в холодильных машинах и установках.
Жидкий аммиак широко применяется в качестве рабочего вещества (хладагента) в холодильных машинах и установках.
Перевозится в сжиженном состоянии под давлением. Предельно допустимые концентрации (ПДК) в воздухе населенных мест: среднесуточная и максимально разовая — 0,2 мг/м3, в рабочем помещении промышленного предприятия — 20 мг/м
Вызывает поражение дыхательных путей. Признаки: насморк, кашель, затрудненное дыхание, удушье, учащается сердцебиение, нарастает частота пульса. Пары сильно раздражают слизистые оболочки и кожные покровы, вызывают жжение, покраснение и зуд кожи, резь в глазах, слезотечение. При соприкосновении жидкого аммиака и его растворов с кожей возникает обморожение, жжение, возможен ожог с пузырями, изъязвления.
Если поражение аммиаком все же произошло, следует немедленно вынести пострадавшего на свежий воздух. Транспортировать надо в лежачем положении. Необходимо обеспечить тепло и покой, дать увлажненный кислород. При отеке легких искусственное дыхание делать нельзя.
Транспортировать надо в лежачем положении. Необходимо обеспечить тепло и покой, дать увлажненный кислород. При отеке легких искусственное дыхание делать нельзя.
В случае аварии необходимо опасную зону изолировать, удалить людей и не допускать никого без средств защиты органов дыхания и кожи. Около зоны следует находиться с наветренной стороны. Место разлива нейтрализуют слабым раствором кислоты, промывают большим количеством воды. Если произошла утечка газообразного аммиака, то с помощью поливомоечных машин, авторазливочных станций, пожарных машин распыляют воду, чтобы поглотить пары.
Зоны заражения АХОВ
В большинстве случаев при аварии и разрушении емкости давление над жидкими веществами падает до атмосферного, АХОВ вскипает и выделяется в атмосферу в виде газа, пара или аэрозоля. Облако газа (пара, аэрозоля) АХОВ, образовавшееся в момент разрушения емкости в пределах первых 3 минут, называется первичным облаком зараженного воздуха. Оно распространяется на большие расстояния. Оставшаяся часть жидкости (особенно с температурой кипения выше 20°С) растекается по поверхности и также постепенно испаряется. Пары (газы) поступают в атмосферу, образуя вторичное облако зараженного воздуха, которое распространяется на меньшее расстояние.
Оставшаяся часть жидкости (особенно с температурой кипения выше 20°С) растекается по поверхности и также постепенно испаряется. Пары (газы) поступают в атмосферу, образуя вторичное облако зараженного воздуха, которое распространяется на меньшее расстояние.
Таким образом, зона заражения АХОВ — это территория, зараженная ядовитыми веществами в опасных для жизни людей пределах (концентрациях).
Глубина зоны распространения зараженного воздуха зависит от концентрации АХОВ и скорости ветра. Например, при ветре 1 м/с за один час облако от места аварии удалится на 5 — 7 км, при 2 м/с — на 10 — 14, а при З м/с — на 16 — 21 км. Значительное увеличение скорости ветра (6-7 м/с и более) способствует его быстрому рассеиванию. Повышение температуры почвы и воздуха ускоряет испарение АХОВ, а следовательно, увеличивает концентрацию его над зараженной территорией. На глубину распространения АХОВ и величину его концентрации в значительной степени влияют вертикальные перемещения воздуха, как мы говорим, погодные условия.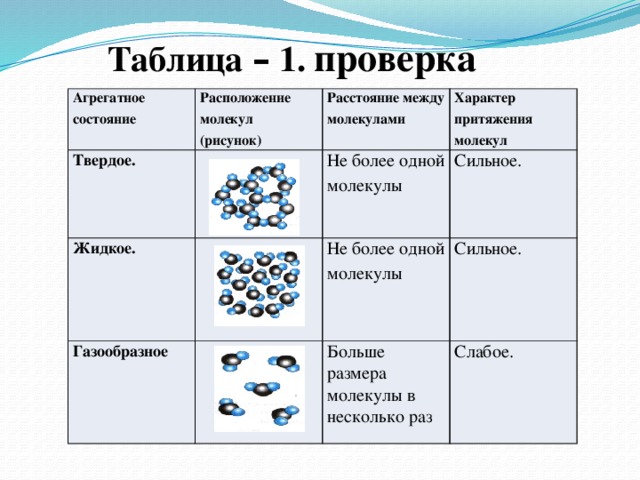
Форма (вид) зоны заражения АХОВ в значительной мере зависит от скорости ветра. Так, например, при скорости менее 0,5 м/с она принимается за окружность, при скорости от 0,6 до 1 м/с — за полуокружность, при скорости от 1,1 м/с до 2 м/ с — за сектор с углом в 90°, при скорости более 2м/с — за сектор с углом в 45°.
Надо иметь в виду, что здания и сооружения городской застройки нагреваются солнечными лучами быстрее, чем расположенные в сельской местности. Поэтому в городе наблюдается интенсивное движение воздуха, связанное обычно с его притоком от периферии к центру по магистральным улицам. Это способствует проникновению АХОВ во дворы, тупики, подвальные помещения и создает повышенную опасность поражения населения. В целом можно считать, что стойкость АХОВ в городе выше, чем на открытой местности.
Вот почему все население, проживающее вблизи химически опасного объекта, должно знать, какие АХОВ используются на этом предприятии, какие ПДК установлены для рабочей зоны производственных помещений и для населенных пунктов, какие меры безопасности требуют неукоснительного соблюдения, какие средства и способы защиты надо использовать в различных аварийных ситуациях.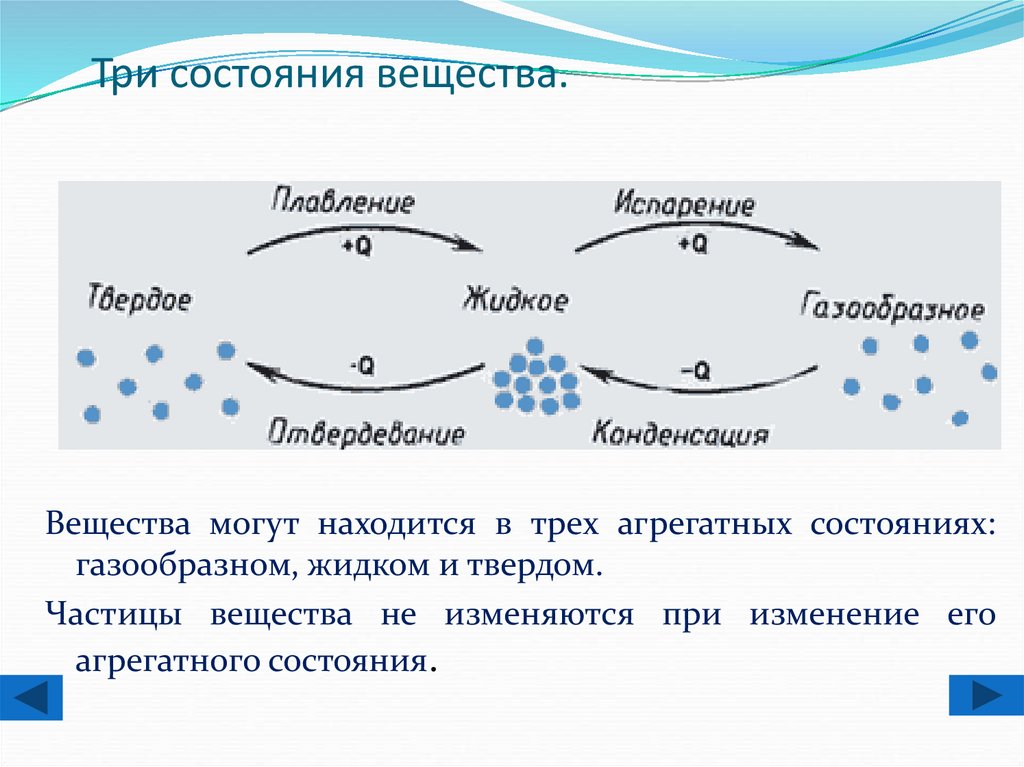
Защита от АХОВ
Защитой от АХОВ служат фильтрующие промышленные и гражданские противогазы, промышленные респираторы, изолирующие противогазы, убежища ГО.
Промышленные противогазы надежно предохраняют органы дыхания, глаза и лицо от поражения. Однако их используют только там, где в воздухе содержится не менее 18% кислорода, а суммарная объемная доля паро- и газообразных вредных примесей не превышает 0,5%.
Недопустимо применять промышленные противогазы для защиты от низкокипящих, плохо сорбирующихся органических веществ (метан, ацетилен, этилен и др.)
Если состав газов и паров неизвестен или их концентрация выше максимально допустимой, применяется только изолирующие противогазы ИП-4 и ИП-5.
Коробки промышленных противогазов строго специализированы по назначению (по составу поглотителей) и отличаются окраской и маркировкой. Некоторые из них изготавливаются с аэрозольными фильтрами, другие без них. Белая вертикальная полоса на коробке означает, что она оснащена фильтром.
Белая вертикальная полоса на коробке означает, что она оснащена фильтром.
Рассмотрим несколько примеров по основным АХОВ. Для защиты от хлора можно использовать промышленные противогазы марок А (коробка коричневого цвета), БКФ (защитного), В (желтого), Г (половина черная, половина желтая), а также гражданские противогазы ГП-5, ГП-7 и детские.
А если их нет? Тогда ватно-марлевую повязку, смоченную водой, а лучше 2%-м раствором питьевой соды.
От аммиака защищает противогаз с другой коробкой, марки КД (серого цвета) и промышленные респираторы РПГ-67КД, РУ-60МКД.
У них две сменных коробки (слева и справа). Они имеют ту же маркировку, что и противогазы. Надо помнить, что гражданские противогазы от аммиака не защищают. В крайнем случае надо воспользоваться ватно-марлевой повязкой, смоченной водой или 5%-м раствором лимонной кислоты.
Для защиты от АХОВ в очаге аварии используются в основном средства индивидуальной защиты кожи (СИЗК) изолирующего типа, общевойсковой защитный комплект ОЗК.
Для населения рекомендуются подручные средства защиты кожи в комплекте с противогазами. Это могут быть обычные непромокаемые накидки и плащи, а также пальто из плотного толстого материала, ватные куртки. Для ног — резиновые сапоги, боты, калоши. Для рук — все виды резиновых и кожаных перчаток и рукавицы.
В случае аварии с выбросом АХОВ убежища обеспечивают надежную защиту. Во-первых, если неизвестен вид вещества или его концентрация слишком велика, можно перейти на полную изоляцию (третий режим), можно также какое-то время находиться в помещении с постоянным объемом воздуха. Во-вторых, фильтропоглотители защитных сооружений препятствуют проникновению хлора, фосгена, сероводорода и многих других ядовитых веществ, обеспечивая безопасное пребывание людей.
В крайнем случае при распространении газов, которые тяжелее воздуха и стелются по земле, как хлор и сероводород, можно спасаться на верхних этажах зданий, плотно закрыв все щели в дверях, окнах, задраив вентиляционные отверстия.
Выходить из зоны заражения нужно в одну из сторон, перпендикулярную направлению ветра, ориентируясь на показания флюгера, развевание флага или любого другого куска материи, наклон деревьев на открытой местности.
Первая помощь пораженным АХОВ
Она складывается из двух частей. Первая — обязательная для всех случаев поражения, вторая — специфическая, зависящая от характера воздействия вредных веществ на организм человека.
Итак, общие требования. Надо как можно скорее прекратить воздействия АХОВ. Для этого необходимо надеть на пострадавшего противогаз и вынести его на свежий воздух, обеспечить полный покой и создать тепло. Расстегнуть ворот, ослабить поясной ремень. При возможности снять верхнюю одежду, которая может быть заражена парами хлора, сероводорода, фосгена или другого вещества.
Специфические. Например, при поражении хлором, чтобы смягчить раздражение дыхательных путей, следует дать вдыхать аэрозоль 0,5%-го раствора питьевой соды. Полезно также вдыхать кислород. Кожу и слизистые промывать 2%-м содовым раствором не менее 15 мин. Из-за удушающего действия хлора пострадавшему передвигаться самостоятельно нельзя. Транспортируют его только в лежачем положении. Если человек перестал дышать, надо немедленно сделать искусственное дыхание методом «изо рта в рот».
Полезно также вдыхать кислород. Кожу и слизистые промывать 2%-м содовым раствором не менее 15 мин. Из-за удушающего действия хлора пострадавшему передвигаться самостоятельно нельзя. Транспортируют его только в лежачем положении. Если человек перестал дышать, надо немедленно сделать искусственное дыхание методом «изо рта в рот».
При поражении аммиаком пострадавшему следует дышать теплыми водяными парами 10%-го раствора ментола в хлороформе, дать теплое молоко с боржоми или содой. При удушье необходим кислород, при спазме голосовой щели — тепло на область шеи, теплые водяные ингаляции. Если произошел отек легких, искусственное дыхание делать нельзя. Слизистые и глаза промывать не менее 15 мин водой или 2%-м раствором борной кислоты. В глаза закапать 2-3 капли 30%-го раствора альбуцида, в нос — теплое оливковое, персиковое или вазелиновое масло. При поражении кожи обливают чистой водой, накладывают примочки из 5%-го раствора уксусной, лимонной или соляной кислоты.
youtube.com/embed/wFU4BpqtQvo» frameborder=»0″ allow=»accelerometer; autoplay; encrypted-media; gyroscope; picture-in-picture» allowfullscreen=»»>Химическая мастерская | Статья в журнале «Школьная педагогика»
Библиографическое описание:Головчанская, Л. Б. Химическая мастерская / Л. Б. Головчанская. — Текст : непосредственный // Школьная педагогика. — 2017. — № 2.1 (9.1). — С. 9-11. — URL: https://moluch.ru/th/2/archive/60/2411/ (дата обращения: 13.11.2022).
Вид деятельности: познавательная
Форма: лаборатория
Направление воспитания: формирование естественно — научного мировоззрения
Направление развития личности: общеинтеллектуальное
Пояснительная записка
Практически каждый ребенок с интересом встречается с новым предметом — химией, предвкушая знакомство с наукой чудес. И это отношение становится основой для познания окружающего мира.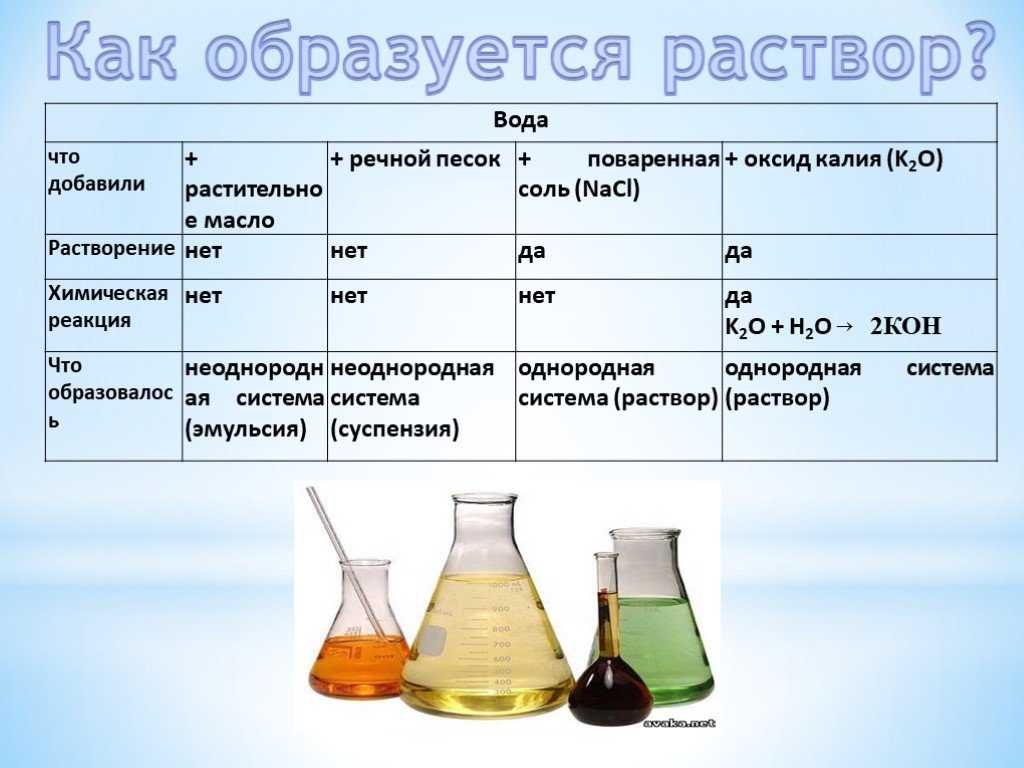 Не увлекаясь высокими теориями, абсолютными понятиями и моделями, без перегрузки курс «Химическая мастерская» позволяет внимательно и ненавязчиво внедрить в сознание учащихся представления о возможностях этой науки, ее доступности и значимости для них.
Не увлекаясь высокими теориями, абсолютными понятиями и моделями, без перегрузки курс «Химическая мастерская» позволяет внимательно и ненавязчиво внедрить в сознание учащихся представления о возможностях этой науки, ее доступности и значимости для них.
В отличие от других подобных курсов, курс «Химическая мастерская» не является системным, в нем не ставится задача формирования системы химических понятий, знаний и умений, раннего изучения основ химии. Предлагаемый курс ориентирован на знакомство и объяснение химических явлений, часто встречающихся в быту, свойств веществ, которые стоят дома на полках кухни и в аптечке. Химические термины и понятия вводятся по мере необходимости объяснить то или иное явление.
Программа внеурочного курса имеет пропедевтическую направленность для учащихся 5 класса и рассчитана на 34 часа.
Цель: развитию умений поиска, анализа и использования знаний.
Задачи:
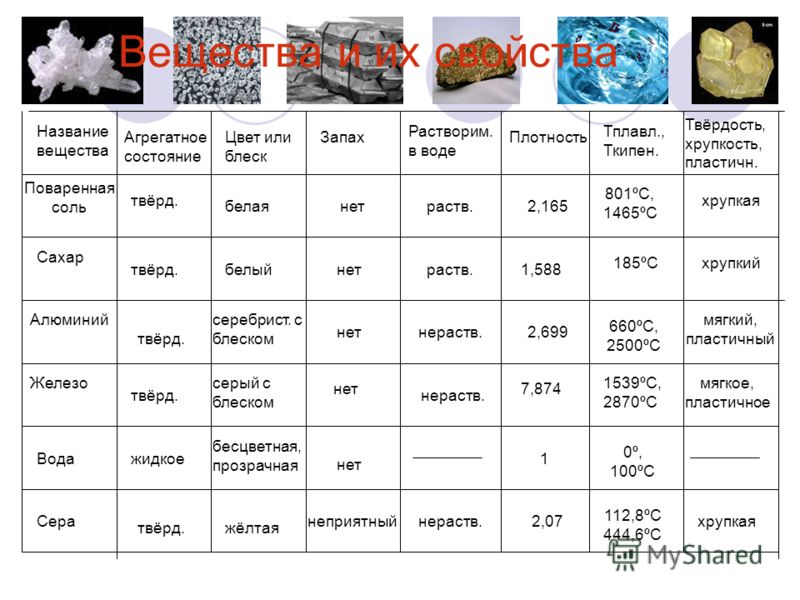
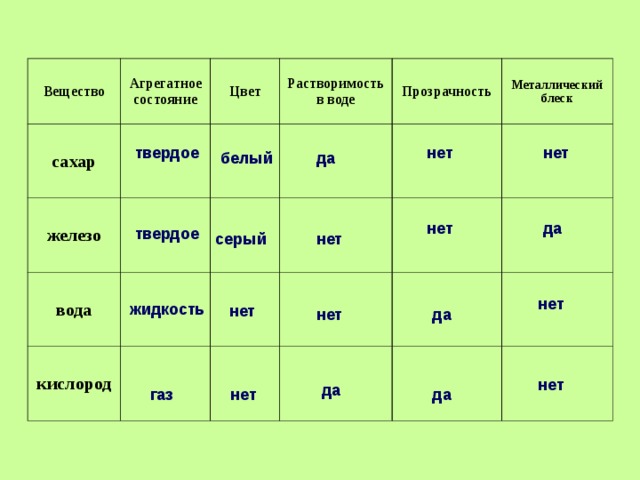
- Развитие умений описывать простейшие физические свойства знакомых веществ (агрегатное состояние, прозрачность, цвет, запах), признаки химической реакции (изменение окраски, выпадение осадка, выделение газа).

- Ознакомление с правилами техники безопасности при работе с веществами.
- Овладение элементарными навыками исследовательской деятельности.
Таблица 1
Учебно-тематический план
№ п/п | Тема | Количество часов | Форма проведения |
1 | Введение в химию | 4 | Беседа Химическая игра |
2 | Оборудование и вещества на кухне | 3 | Наблюдение Беседа |
3 | Что мы пьем? | 12 | Эксперимент Химическая игра |
4 | Что мы едим? | 13 | Эксперимент Практикум |
5 | Делаем уборку на кухне | 2 | Проект |
Содержание тем
Тема 1. Введение вхимию (4 часа)
Введение вхимию (4 часа)
Предмет химии. Вещества. Молекулы. Атомы. Физические и химические явления.
Практическая работа: приемы обращения с лабораторным оборудованием
Тема 2. Оборудование ивещества на кухне (3 часа)
Газовая плита. Природный газ, метан. Горение. Строение пламени. Кислород. Горение веществ в кислороде и воздухе. Реакции соединения. Способы прекращения горения. Углекислый газ. Простые и сложные вещества. Моделирование молекул кислорода, углекислого газа, метана.
Демонстрации: получение кислорода, обнаружение кислорода и углекислого газа.
Лабораторные опыты: изучение строения пламени.
Тема 3. Что мы пьем? (12 часов)
Вода. Реакция разложения воды.Моделирование молекулкислорода. водорода, воды. Реакция разложения на примере воды. Отличие реакций соединения и разложения. Вода — идеальный растворитель. Растворимость веществ в воде.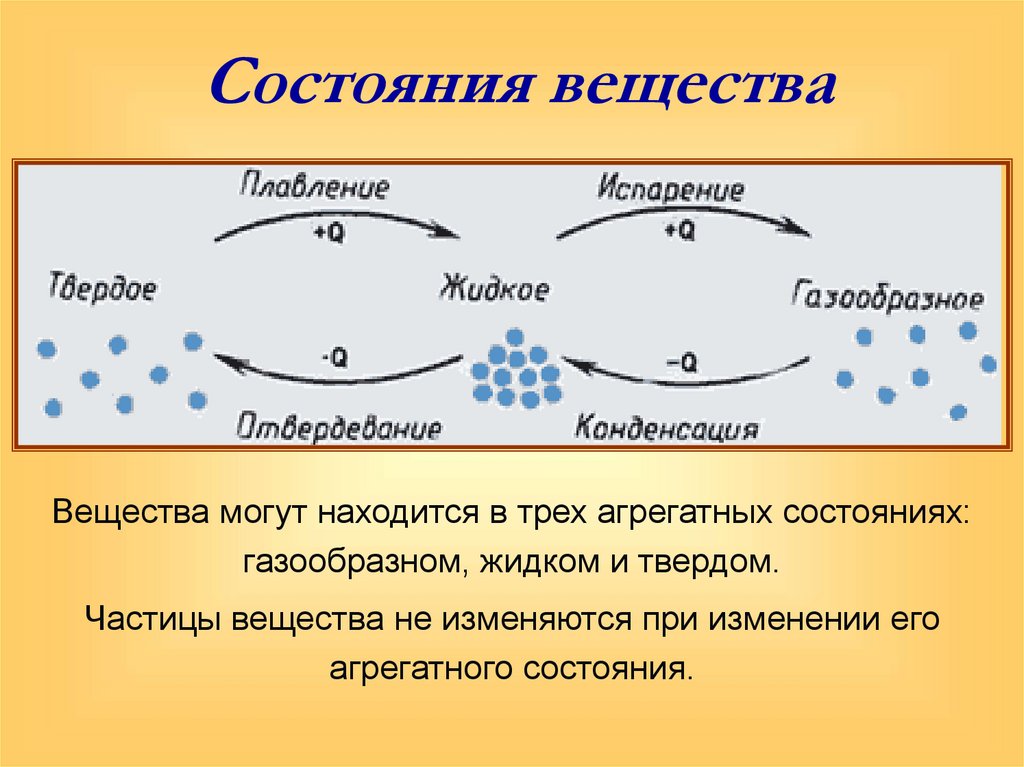 Минеральная и газированная вода. Чай и кофе. Молоко, скисание молока, молочная кислота, молочные продукты (простокваша, кефир). Чистые вещества и смеси.
Минеральная и газированная вода. Чай и кофе. Молоко, скисание молока, молочная кислота, молочные продукты (простокваша, кефир). Чистые вещества и смеси.
Лабораторные опыты:
– растворение веществ в воде (суспензия мыла, эмульсия растительного масла, раствор поваренной соли):
– выпаривание раствора минеральной воды;
– обнаружение молочной кислоты в кефире, белков в молоке.
Практическая работа: очистка поваренной соли
Тема 4. Что мы едим? (13 часов)
Хлеб. Тесто. Дрожжи. Углеводы. Соли; поваренная соль и питьевая сода.
Ягоды и фрукты. Глюкоза. Моделирование молекулы глюкозы. Брожение — химический процесс. Картофель, крахмал, углеводы.
Жиры. Растительные и животные жиры. Сливочное масло, маргарин.
Яйцо. Мясо. Рыба. Белки.
Демонстрации: пористое строение теста.
Лабораторные опыты:
– обнаружение крахмала, глюкозы в хлебе;
– взаимодействие соды с уксусной кислотой;
Тема 5.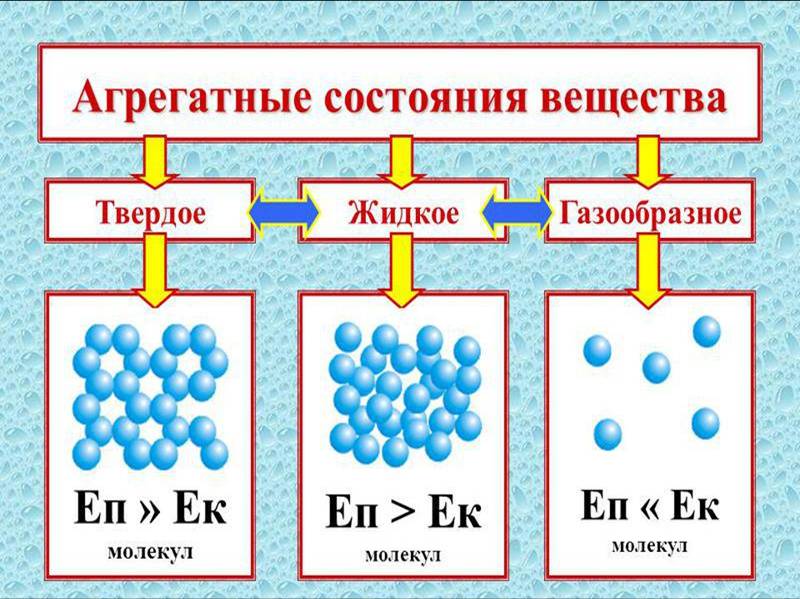 Делаем уборку на кухне (2 часа)
Делаем уборку на кухне (2 часа)
Чистящие средства: сода, мыло, кислоты, нашатырный спирт.
Демонстрации: получение мыла.
Лабораторные опыты:
– растворение накипи и ржавчины кислотой;
– обнаружение щелочной и кислой среды индикатором.
Контрольно-измерительные материалы
- Конкурсы презентаций по темам: «Вещества на кухне», «Вода», «Что мы пьём?» «Белки. Жиры. Углеводы», «Глюкоза. Крахмал», «Чистящие средства».
- Конкурс «Юный химик».
- Экскурсия в магазин.
- Викторина по теме «Вода — источник жизни».
Вопросы викторины:
Загадки:
1. Что видно, когда ничего не видно?
2. Темным облаком летела,
Опустилась птицей белой.
Превратилась в человечка,
Постояла у крылечка,
Покатилась кувырком
И запела ручейком.
3. На дворе переполох –
С неба сыплется горох.
Съела шесть горошин Нина –
У неё теперь ангина.
4.Без пути и без дороги
Ходит самый длинноногий,
В тучах прячется. Во мгле.
Только ноги на земле.
5. Без крыльев летят,
Без ног бегут,
Без паруса плывут.
6. Не снег и не лёд,
А серебром деревья уберёт.
«Что? Почему? Зачем? Как?»
- Назовите восемь наименований состояний воды, принятых в метеорологии.
- Отличается ли молекула водяного пара от молекулы воды?
- Можно ли высушить бельё на морозе? Почему?
- Какой водопад считается самым мощным в мире?
- В каком органе человека содержится наибольшее количество воды, а в каком — наименьшее?
- Что означает выражение «Выйти сухим из воды»?
- Почему говорят «Как с гуся вода?»
- Правда ли. что вода в море соленая, от того, что в ней плавает селёдка?
- Какой воздух тяжелее сухой или влажный?»
- Что налито в стакане? Почему яйцо не тонет?
Литература:
- Аспицкая А.
 Ф., Шиляева Л. А. Программа пропедевтического курса химии для 5–7 классов. Пермь, 1995
Ф., Шиляева Л. А. Программа пропедевтического курса химии для 5–7 классов. Пермь, 1995 - Алексинский В. Н. Занимательные опыты по химии. М.: Просвещение, 1980
- Кукушкин Ю. Н. Химия вокруг нас. М.: Высшая школа, 1992
- Штремплер Г. И. Химия на досуге. М.: Просвещение, 1993
- Ольгин О. Н. Опыты без взрывов. М.: Химия, 1986
- Юдин А. М. Химия в нашем доме. М.: Химия.1990
Основные термины (генерируются автоматически): вод, поваренная соль, углекислый газ, Вещество, кухня, молочная кислота, практическая работа, химическая игра, час.
Интеграционные исследования томских ученых в различных…
вод, поваренная соль, углекислый газ, час, кухня, Вещество, химическая игра, практическая работа, молочная кислота. Определение содержание свободной и связанной влаги в тесте…
Определение содержание свободной и связанной влаги в тесте…
В данной работе рассмотрен опыт по химическому взаимодействию лимонной кислоты и гидрокарбоната натрия (пищевой соды).
Угольная кислота практически сразу распадается на воду и углекислый газ
Дидактические
игры на современном уроке химииА. Угарный газ. 2. Оксид углерода (IV). Б. Поваренная соль.
Преподавание курса химии и практические работы по решению… При действии ее на вещество пробирки 1 выделяется оксид углерода (IV), что доказывает наличие карбоната натрия; приливание.
Использование электролизованных растворов
поваренной соли…Оценивая влияние физических факторов воды на процессы деструкции токсина продуктами электролиза поваренной соли, следует отметить что наибольшее значение имеет цветность воды.
Эффективное использование отходов
химических опытов на…При изучении водорода, воды и растворов, оксидов, гидроксидов, кислот и солей проводится большое число лабораторных опытов, при
Преподавание курса химии и практические работы по решению…
Использование электролизованных растворов поваренной соли…
Химия варки древних стекол на зольной шихте | Статья в журнале. ..
..Хлористый натрий (NaCl, поваренная соль) реагирует с SiO2 лишь в присутствии паров воды, еле заметно
Для стекловарения ценна зола с углекислыми солями щелочных металлов, а
Химические опыты с пищевой содой и лимонной кислотой… Пищевая сода (питьевая сода…
Усовершенствование процесса получения цианистого натрия
HCN получают путем сплавления черного цианоплава с поваренной солью, который далее выщелачивают водой.
Разложение бикарбоната натрия и удаление избытка аммиака и углекислого газа паром
Цветовые эффекты в химических опытах с гидроксидом натрия.
О процессах таяния снега и кристаллизации
воды под…Практическая значимость работы очевидна.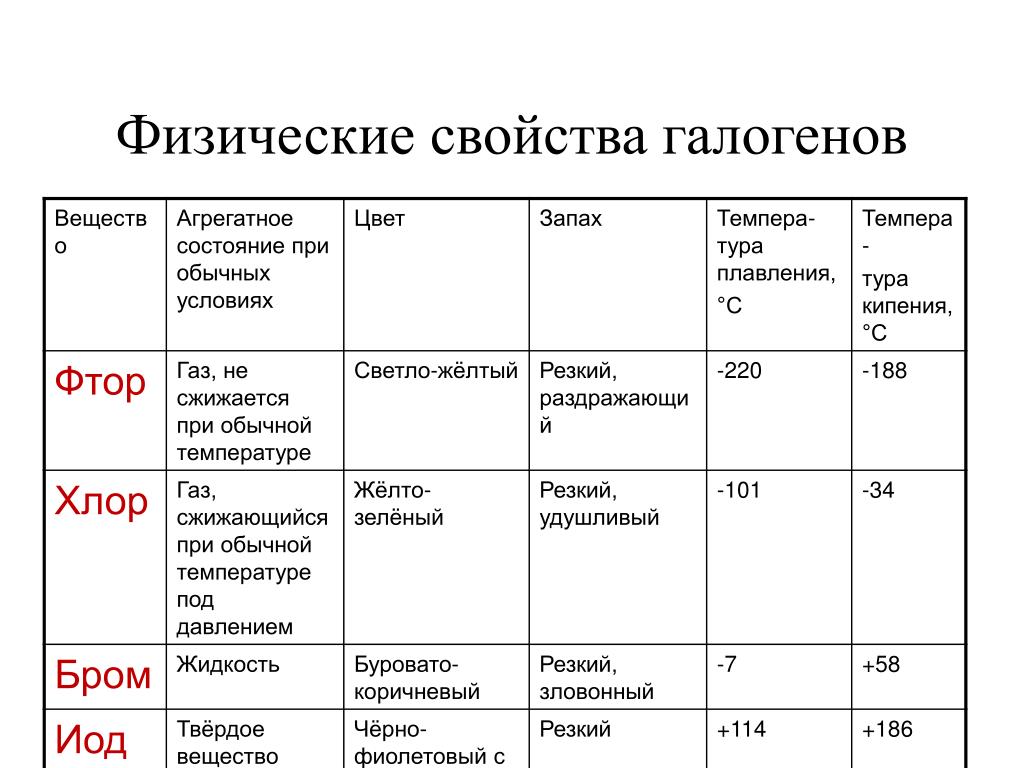 Люди часто и давно используют различные способы, чтобы растаять замерзшую воду.
Люди часто и давно используют различные способы, чтобы растаять замерзшую воду.
В стаканы засыпаются реагенты в количестве 2 чайных ложек: 1 — лимонная кислота, 2 — пищевая сода, 3 — поваренная соль, 4 — сахар, 5…
Разработка технологии бездрожжевого хлеба | Статья в журнале…
Гетероферментативные бактерии, которые наряду с молочной кислотой образуют значительное количество летучих кислот, в том числе уксусной кислоты, этилового спирта, углекислого газа и других соединений
В дежу дозируют закваску, муку, воду, сахар и соль.
Vanishing Baking Soda — Scientific American
Share on Facebook
Share on Twitter
Share on Reddit
Share on LinkedIn
Share via Email
Print
Ключевые понятия
Химия
Газы
Химическая реакция
Термическое разложение
Введение
Пищевая сода не только отлично подходит для приготовления пищи, но и является полезным химическим веществом для научных проектов. Вы, наверное, слышали и, возможно, даже использовали реакцию пищевой соды и уксуса, чтобы заставить самодельные вулканы извергаться, запускать ракеты из бутылок в воздух или обнаруживать кислоты и щелочи. Однако есть еще много химических реакций, которые вы можете исследовать с помощью пищевой соды. Одна из них называется реакцией разложения, благодаря которой пищевая сода худеет! Хотите узнать, как это работает?
Вы, наверное, слышали и, возможно, даже использовали реакцию пищевой соды и уксуса, чтобы заставить самодельные вулканы извергаться, запускать ракеты из бутылок в воздух или обнаруживать кислоты и щелочи. Однако есть еще много химических реакций, которые вы можете исследовать с помощью пищевой соды. Одна из них называется реакцией разложения, благодаря которой пищевая сода худеет! Хотите узнать, как это работает?
Фон
Химические вещества могут подвергаться множеству различных реакций, таких как реакции синтеза, в результате которых создаются новые вещества, или реакции горения, при которых вещество обычно взаимодействует с кислородом и вырабатывает энергию в виде тепла. Другим типом реакции является реакция разложения, противоположная реакции синтеза. Когда химическое вещество разлагается, оно распадается на два или более отдельных соединения. Большинство химических соединений довольно стабильны и самопроизвольно не разлагаются. Вы должны приложить много энергии, чтобы разорвать их химические связи.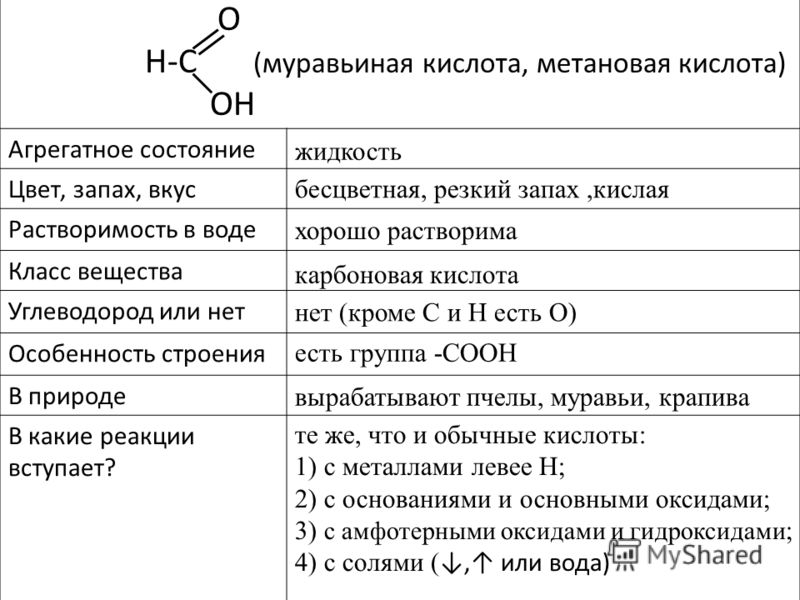 Однако когда химические вещества подвергаются воздействию достаточного количества энергии, которая может быть в форме тепла, излучения, электричества или света, они разлагаются.
Однако когда химические вещества подвергаются воздействию достаточного количества энергии, которая может быть в форме тепла, излучения, электричества или света, они разлагаются.
Реакции разложения являются причиной того, что некоторые химические вещества или отпускаемые по рецепту лекарства хранятся в бутылках из темного стекла. Часто вы не хотите, чтобы химическое вещество разлагалось, потому что его химическая природа изменится. Темное стекло уменьшает количество света, попадающего на химическое вещество или лекарство, и, следовательно, предотвращает разложение химического вещества под действием света.
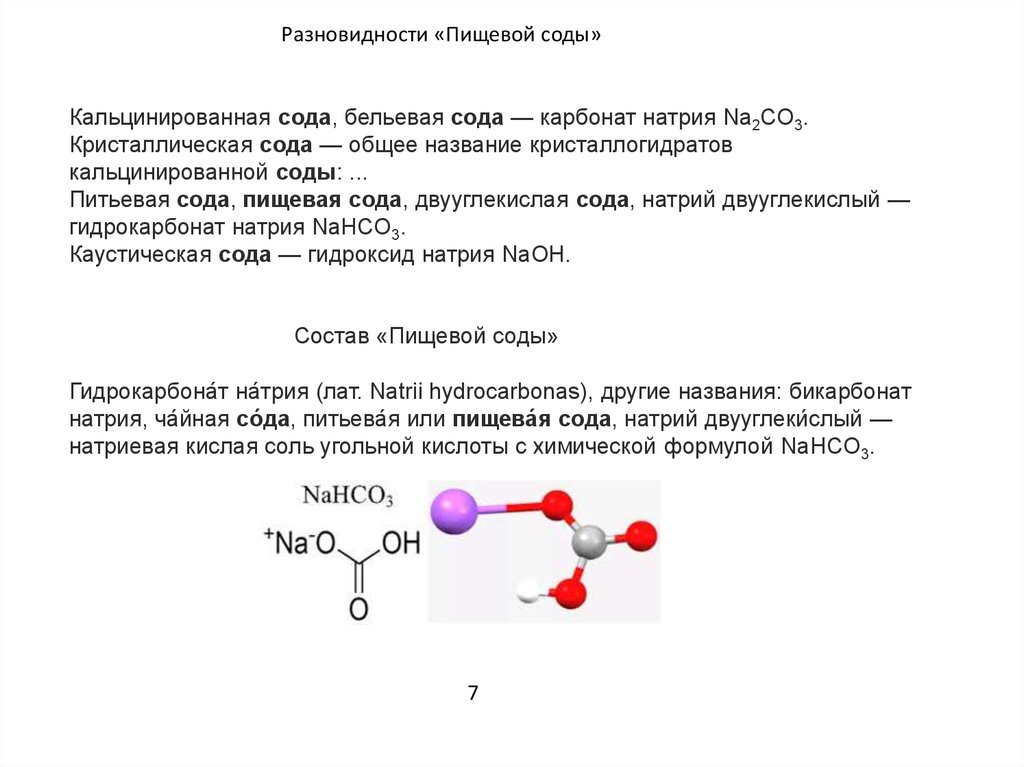
Пищевая сода или бикарбонат натрия (NaHCO 3 ) представляет собой химическое вещество, которое может подвергаться реакции разложения при нагревании. При температуре выше 176 градусов по Фаренгейту (80 градусов по Цельсию) бикарбонат натрия начинает распадаться на три соединения, образуя карбонат натрия (Na 2 CO 3 ), воду (H 2 O) и диоксид углерода (CO 2 ). Вы используете эту реакцию каждый раз, когда готовите и выпекаете. Вырабатываемый углекислый газ заставляет выпечку подниматься вверх! Чем выше температура бикарбоната натрия, тем быстрее он будет разлагаться. Только карбонат натрия останется в виде твердого продукта. И углекислый газ, и вода газообразны при высокой температуре, а это значит, что они растворяются в окружающем воздухе. Вы действительно можете измерить эту потерю — возьмите немного пищевой соды и узнайте, как это сделать, в этом упражнении!
Вы используете эту реакцию каждый раз, когда готовите и выпекаете. Вырабатываемый углекислый газ заставляет выпечку подниматься вверх! Чем выше температура бикарбоната натрия, тем быстрее он будет разлагаться. Только карбонат натрия останется в виде твердого продукта. И углекислый газ, и вода газообразны при высокой температуре, а это значит, что они растворяются в окружающем воздухе. Вы действительно можете измерить эту потерю — возьмите немного пищевой соды и узнайте, как это сделать, в этом упражнении!
Материалы
- Две жаропрочные тарелки
- Ложка
- Пищевая сода
- Цифровая шкала (желательно с шагом 0,1 грамма)
- Духовка
- Прихватки для духовки
- Помощник для взрослых
- Термостойкая поверхность
- Таймер
- Бумага и ручка или карандаш
Подготовка
- Разогрейте кухонную духовку до 200 градусов F (около 93 градуса С).

- Включите весы и обнулите их.
- Положите первую тарелку на весы. Запишите его точную массу.
- Затем снова обнулите весы и добавьте ложкой 15 г пищевой соды.
- Добавьте массу пустой тарелки к массе пищевой соды, чтобы рассчитать их общий вес. Запишите свой результат на листе бумаги.
- Повторите эти действия со второй пластиной. Обязательно запомните, какая тарелка какая. Вы можете пометить их, если хотите.
Процедура
- Как только духовка достигнет заданной температуры (200 градусов по Фаренгейту), пусть ваш взрослый помощник поместит в духовку первую тарелку с пищевой содой. Отметьте, какой именно.
- Установите таймер на 15 минут и оставьте тарелку в духовке, пока не сработает таймер. Как вы думаете, что произойдет с пищевой содой в духовке?
- Попросите вашего взрослого помощника осторожно вынуть тарелку с пищевой содой из духовки. Обязательно наденьте прихватки! Как выглядит пищевая сода? Изменил ли он свой внешний вид при нагревании?
- Установите пластину на термостойкую поверхность рабочего места и дайте ей остыть в течение 5–10 минут.

- Установите духовку на 400 градусов по Фаренгейту (около 204 градусов по Цельсию).
- Снова включите весы, обнулите их и установите на весы остывшую тарелку с пищевой содой. Запишите его точную массу. Какова масса по сравнению с массой до того, как вы поставите тарелку с пищевой содой в духовку? Он стал тяжелее, легче или остался прежним?
- Когда духовка достигнет новой заданной температуры, ваш взрослый помощник поместит вторую тарелку с пищевой содой внутрь.
- Снова установите таймер на 15 минут и оставьте пищевую соду в духовке на все время. Как вы думаете, вы получите другой результат при температуре 400 градусов по Фаренгейту? Что будет с пищевой содой на этот раз?
- Через 15 минут ваш взрослый помощник осторожно вытащит из духовки тарелку с пищевой содой в прихватках. Как на этот раз выглядит пищевая сода? Он изменил цвет или все еще выглядит так же?
- Отложите в сторону и дайте пластине остыть в течение 5-10 минут.

- Затем снова включите весы, обнулите их и положите на весы вторую остывшую пластину. Запишите его точную массу. Как изменится масса пищевой соды (плюс тарелка) при нагревании до 400 градусов по Фаренгейту в течение 15 минут?
- Рассчитайте разницу масс пищевой соды до и после нагревания при 200° и 400°F. Вычтите массу плиты и пищевой соды после нагревания из массы плиты и пищевой соды до нагревания. Сколько массы было потеряно или прибавлено в процессе нагревания? Была ли разница между обеими температурами?
- Можно также выразить изменение массы пищевой соды, рассчитав ее потерю массы в процентах (разность масс пищевой соды до и после нагревания, умноженная на 100 и затем поделенная на начальную массу пищевой соды). Какой процент по массе потеряла или увеличила пищевая сода в процессе нагревания при обеих температурах? Было ли это то же самое? Если нет, можете объяснить разницу?
- Extra : Вы можете проверить, как изменяется масса пищевой соды при других температурах.
 Повторите тот же тест, но установите духовку на другую температуру (например, 250, 300 или 350 градусов по Фаренгейту). Как вы думаете, ваши результаты будут разными для каждой температуры или одинаковыми? Почему?
Повторите тот же тест, но установите духовку на другую температуру (например, 250, 300 или 350 градусов по Фаренгейту). Как вы думаете, ваши результаты будут разными для каждой температуры или одинаковыми? Почему? - Extra : Можете ли вы найти на кухне другие вещества, которые могут разлагаться? Узнайте, при каких температурах разлагаются эти соединения и, если возможно (и безвредно), испытайте это на себе!
Наблюдения и результаты
Вы видели, как ваша пищевая сода похудела? Вы должны были иметь — по крайней мере, для более высокой температуры в 400 градусов по Фаренгейту. Для более низкой температуры ваша масса пищевой соды после нагревания, вероятно, была такой же (или почти такой же), как до того, как вы поместили ее в духовку. Пищевая сода начинает разлагаться при температуре около 176 градусов по Фаренгейту. Однако при этих температурах разложение будет относительно медленным. Пятнадцати минут в духовке при температуре 200 градусов по Фаренгейту недостаточно, чтобы значительно разложить пищевую соду.
При повышении температуры до 400 градусов по Фаренгейту реакция разложения пойдет намного быстрее. Пятнадцати минут достаточно, чтобы разложить пищевую соду на карбонат натрия, воду и углекислый газ. Газообразные продукты (вода и углекислый газ) будут выходить в воздух, поэтому полученный продукт должен быть значительно легче того, что вы положили в печь.
Внешний вид пищевой соды не изменится ни при одной температуре. Хотя вы сделаете новый продукт — карбонат натрия — из пищевой соды во время реакции разложения, он все равно будет выглядеть так же. Оба вещества представляют собой белый порошок.
Очистка
Обязательно выключите духовку. Дайте обеим пластинам остыть до комнатной температуры. Затем вы можете выбросить использованную пищевую соду в мусорное ведро. Вымойте руки теплой водой с мылом и очистите рабочее место.
Еще для изучения
Термическое разложение от BBC Bitesize
Химия для детей, химические реакции от Ducksters Education Site
Уравнение разложения бикарбоната натрия или пищевой соды от ThoughtCo.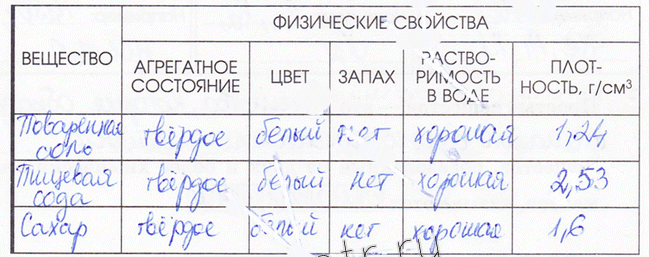
Это задание было предложено вам в сотрудничестве с Science Buddies
ОБ АВТОРАХ
ФОН: | |||||||||

 Ф., Шиляева Л. А. Программа пропедевтического курса химии для 5–7 классов. Пермь, 1995
Ф., Шиляева Л. А. Программа пропедевтического курса химии для 5–7 классов. Пермь, 1995

 Повторите тот же тест, но установите духовку на другую температуру (например, 250, 300 или 350 градусов по Фаренгейту). Как вы думаете, ваши результаты будут разными для каждой температуры или одинаковыми? Почему?
Повторите тот же тест, но установите духовку на другую температуру (например, 250, 300 или 350 градусов по Фаренгейту). Как вы думаете, ваши результаты будут разными для каждой температуры или одинаковыми? Почему? 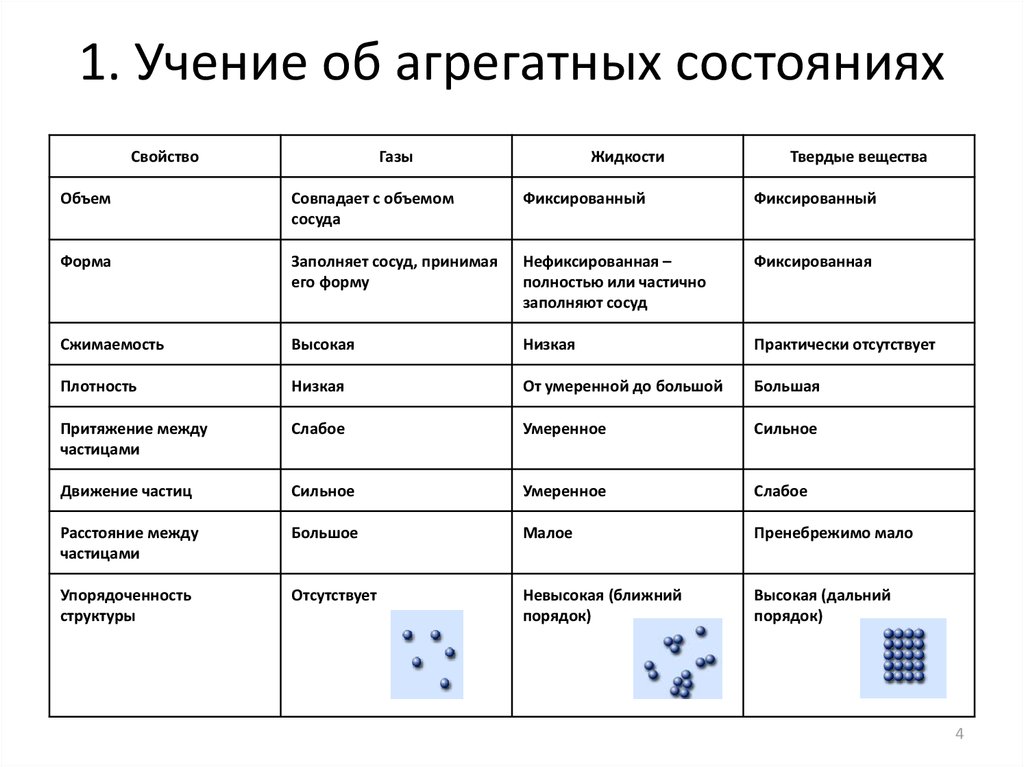 раскраска. Если у вас нет глины, вы можете провести
поэкспериментируйте в пластиковой чашке, колбе или пробирке. Если вы незнакомы
с реакцией уксуса и пищевой соды, вы можете попробовать ее несколько раз.
раз, пока вы не почувствуете необходимое количество реагентов.
Сформируйте из глины «вулкан» в качестве модели для ваших учеников.
Убедитесь, что вы оставили место наверху, чтобы положить примерно ложку выпечки.
сода.
раскраска. Если у вас нет глины, вы можете провести
поэкспериментируйте в пластиковой чашке, колбе или пробирке. Если вы незнакомы
с реакцией уксуса и пищевой соды, вы можете попробовать ее несколько раз.
раз, пока вы не почувствуете необходимое количество реагентов.
Сформируйте из глины «вулкан» в качестве модели для ваших учеников.
Убедитесь, что вы оставили место наверху, чтобы положить примерно ложку выпечки.
сода. 